Lei de Charles
Storyboard 
A lei de Charles estabelece que o quociente entre o volume (V) e la temperatura absoluta (T) de um gás é constante, desde que a pressão e a quantidade de mols permaneçam inalteradas.
Isso implica que o volume (V) varia de forma proporcional a la temperatura absoluta (T).
ID:(1473, 0)
Mecanismos
Iframe 
A lei de Charles estabelece que o volume de um gás é diretamente proporcional à sua temperatura quando a pressão é mantida constante. Isso significa que, à medida que a temperatura de um gás aumenta, seu volume também aumenta, desde que a pressão permaneça a mesma. Inversamente, se a temperatura diminui, o volume também diminui. Essa relação é fundamental para entender o comportamento dos gases e é frequentemente observada ao aquecer ou resfriar um gás em um recipiente flexível, como um balão, onde a mudança de temperatura resulta em uma mudança notável de volume.
Mecanismos
ID:(15255, 0)
Variação de volume e temperatura
Conceito 
A geração de la pressão (p) ocorre quando as partículas de gás colidem com a superfície do recipiente de gás. Cada colisão transmite um momento igual ao dobro de la massa molar (m) vezes la velocidade média de uma partícula (\bar{v}). Além disso, é importante considerar o fluxo de partículas em direção à superfície, que depende de la concentração de partículas (c_n), mas também de la velocidade média de uma partícula (\bar{v}), com o qual se deslocam. Portanto,
p \propto c_n v \cdot m v = c_n m v^2
O fluxo de partículas e a transmissão do momento são representados no seguinte gráfico:

Dado que la massa molar (m) vezes la velocidade média de uma partícula (\bar{v}) ao quadrado é proporcional à energia, e esta à La temperatura absoluta (T),
mv^2 \propto E \propto T
e, dado que o número de partículas (N) é constante, la concentração de partículas (c_n) é inversamente proporcional a o volume (V):
c_n \propto \displaystyle\frac{1}{V}
Como la pressão (p) é constante, temos:
p \propto \displaystyle\frac{T}{V}
o que implica:
V \propto T
ID:(15689, 0)
Significado de temperatura absoluta
Descrição 
A temperatura corresponde à energia térmica (movimento) contida em um objeto.
Uma vez que a energia é sempre positiva, escalas de temperatura como Celsius e Fahrenheit, que podem assumir valores negativos, podem parecer não intuitivas. No entanto, a relação entre energia e temperatura leva à conclusão de que deve existir uma temperatura mínima, conhecida como temperatura zero absoluto, na qual a energia de um sistema de partículas é nula.
Além disso, em 1802, Gay-Lussac observou que nos gases existe uma relação proporcional entre o volume e a temperatura. Essa proporção implica que um gás atingiria um volume de zero a uma temperatura de -273,15 graus Celsius (de acordo com medições modernas), o que é conhecido como temperatura absoluta zero:
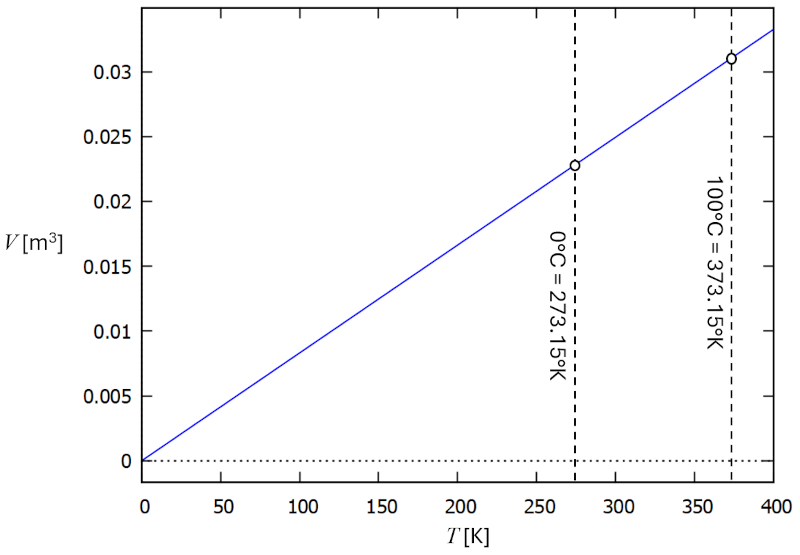
Isso implica na existência de tal escala, que foi denominada a escala de temperatura absoluta medida em graus Kelvin. Outras escalas, como as temperaturas t em graus Celsius ou Fahrenheit, podem ser convertidas para
Celsius:
T = 273.15 + t
Fahrenheit:
T = 255.37 + \displaystyle\frac{5}{9} t
ID:(111, 0)
Igualdade das diferenças de temperatura Celsius e Kelvin
Conceito 
La diferença de temperatura em graus Celsius (\Delta t), combinado com la temperatura em graus Celsius no estado 1 (t_1) e la temperatura em graus Celsius no estado 2 (t_2), resulta em:
\Delta t = t_2 - t_1
Se expressarmos ambas as temperaturas em graus Kelvin, temos que la temperatura no estado 1 (T_1) é igual a:
T_1 = t_1 + 273.15 , \text{K}
e la temperatura no estado 2 (T_2) é igual a:
T_2 = t_2 + 273.15 , \text{K}
Portanto, a diferença de temperaturas em Kelvin, denominada la diferença de temperatura (\Delta T), é calculada como:
\Delta T=T_2-T_1=t_2-t_1=\Delta t
Isso implica:
| \Delta T = \Delta t |
O que significa que a diferença entre as temperaturas em graus Celsius e Kelvin permanece a mesma.
ID:(15694, 0)
Relação temperatura x volume
Descrição 
Em um gás, quando la pressão (p) e o número de partículas (N) são mantidos constantes, observa-se que o volume (V) e la temperatura absoluta (T) variam de forma proporcional. Quando o volume (V) diminui, la temperatura absoluta (T) também diminui, e vice-versa,
V \propto T
como mostrado no seguinte gráfico:

A lei de Charles [1] afirma que, com la pressão (p) e o número de partículas (N) constantes, o volume (V) e la temperatura absoluta (T) são diretamente proporcionais.
Isso pode ser expresso com la constante da lei de Charles (C_c) da seguinte forma:
| \displaystyle\frac{ V }{ T } = C_c |
![]() [1] "Sur la dilatação dos gases e vapores" (Sobre a expansão dos gases e vapores), Jacques Charles, Academia Francesa de Ciências (1787)
[1] "Sur la dilatação dos gases e vapores" (Sobre a expansão dos gases e vapores), Jacques Charles, Academia Francesa de Ciências (1787)
ID:(9529, 0)
Jacques Charles
Descrição 
Jacques Charles, nascido em 12 de novembro de 1746 e falecido em 7 de abril de 1823, foi um físico, inventor e aeronauta francês. Ele é conhecido principalmente por seu trabalho pioneiro no campo da aeronáutica e por suas descobertas relacionadas ao comportamento dos gases. Em 1783, realizou o primeiro voo tripulado em um balão cheio de hidrogênio, em parceria com o químico Nicolas-Louis Robert. Esse voo bem-sucedido marcou um marco importante na história da aviação. Charles também fez contribuições importantes para a compreensão das leis dos gases, incluindo a Lei de Charles, que descreve a relação entre o volume e a temperatura de um gás a pressão constante.
Nota: A Lei de Charles foi tornada pública por Joseph Louis Gay-Lussac, que a atribuiu a Jacques Charles, citando um artigo não publicado.

ID:(1656, 0)
Mudança de estado de um gás ideal de acordo com a lei de Charles
Conceito 
A lei de Charles estabelece que, com la pressão (p) constante, a proporção de o volume (V) com la temperatura absoluta (T) é igual a la constante da lei de Charles (C_c):
| \displaystyle\frac{ V }{ T } = C_c |
Isso significa que se um gás passa de um estado inicial (o volume no estado i (V_i) e la temperatura no estado inicial (T_i)) para um estado final (o volume no estado f (V_f) e la temperatura no estado final (T_f)), mantendo la pressão (p) constante, ele deve sempre obedecer à lei de Charles:
\displaystyle\frac{V_i}{T_i} = C_c = \displaystyle\frac{V_f}{T_f}
Portanto, temos:
| \displaystyle\frac{ V_i }{ T_i }=\displaystyle\frac{ V_f }{ T_f } |
ID:(15692, 0)
Equivalente à lei de Charles para densidades
Conceito 
Se em um processo isotérmico, no qual o conteúdo permanece constante, tivermos que la temperatura no estado inicial (T_i), la temperatura no estado final (T_f), o volume no estado i (V_i) e o volume no estado f (V_f) estão relacionados pela seguinte equação:
| \displaystyle\frac{ V_i }{ T_i }=\displaystyle\frac{ V_f }{ T_f } |
Então, podemos introduzir la densidade (\rho), que, juntamente com la massa (M) e o volume (V), satisfaz:
| \rho \equiv\displaystyle\frac{ M }{ V } |
Isso nos leva a la densidade no estado i (\rho_i) e la densidade no estado f (\rho_f) como:
| \rho_i T_i = \rho_f T_f |
ID:(15693, 0)
Modelo
Top 
Parâmetros
Variáveis
Cálculos
Cálculos
Cálculos
Equações
\rho_i \equiv\displaystyle\frac{ M }{ T_i }
rho = M / V
\rho_f \equiv\displaystyle\frac{ M }{ T_f }
rho = M / V
\rho_i T_i = \rho_f T_f
rho_1 * T_1 = rho_2 * T_2
\displaystyle\frac{ V_i }{ T_i } = C_c
V / T = C_c
\displaystyle\frac{ V_f }{ T_f } = C_c
V / T = C_c
\displaystyle\frac{ V_i }{ T_i }=\displaystyle\frac{ V_f }{ T_f }
V_i / T_i = V_f / T_f
ID:(15314, 0)
Lei de Charles (1)
Equação 
A lei de Charles estabelece uma relação entre o volume (V) e la temperatura absoluta (T), indicando que sua proporção é igual a la constante da lei de Charles (C_c), da seguinte forma:
ID:(583, 1)
Lei de Charles (2)
Equação 
A lei de Charles estabelece uma relação entre o volume (V) e la temperatura absoluta (T), indicando que sua proporção é igual a la constante da lei de Charles (C_c), da seguinte forma:
ID:(583, 2)
Mudança de estado de um gás ideal de acordo com a lei de Charles
Equação 
Se um gás passa de um estado inicial (i) para um estado final (f) com la pressão (p) constante, então para o volume no estado i (V_i), o volume no estado f (V_f), la temperatura no estado inicial (T_i) e la temperatura no estado final (T_f) é válido:
A lei de Charles estabelece que, com la pressão (p) constante, a proporção de o volume (V) com la temperatura absoluta (T) é igual a la constante da lei de Charles (C_c):
| \displaystyle\frac{ V }{ T } = C_c |
Isso significa que se um gás passa de um estado inicial (o volume no estado i (V_i) e la temperatura no estado inicial (T_i)) para um estado final (o volume no estado f (V_f) e la temperatura no estado final (T_f)), mantendo la pressão (p) constante, ele deve sempre obedecer à lei de Charles:
\displaystyle\frac{V_i}{T_i} = C_c = \displaystyle\frac{V_f}{T_f}
Portanto, temos:
| \displaystyle\frac{ V_i }{ T_i }=\displaystyle\frac{ V_f }{ T_f } |
ID:(3492, 0)
Massa e Densidade (1)
Equação 
La densidade (\rho) é definido como a relação entre la massa (M) e o volume (V), expressa como:
Essa propriedade é específica do material em questão.
ID:(3704, 1)
Massa e Densidade (2)
Equação 
La densidade (\rho) é definido como a relação entre la massa (M) e o volume (V), expressa como:
Essa propriedade é específica do material em questão.
ID:(3704, 2)
Equivalente à lei de Charles para densidades
Equação 
Para os estados iniciais (la densidade no estado i (\rho_i), o volume no estado i (V_i)) e finais (la densidade no estado f (\rho_f), o volume no estado f (V_f)), a lei de Charles é obtida da seguinte forma:
Se em um processo isotérmico, no qual o conteúdo permanece constante, tivermos que la temperatura no estado inicial (T_i), la temperatura no estado final (T_f), o volume no estado i (V_i) e o volume no estado f (V_f) estão relacionados pela seguinte equação:
| \displaystyle\frac{ V_i }{ T_i }=\displaystyle\frac{ V_f }{ T_f } |
Então, podemos introduzir la densidade (\rho), que, juntamente com la massa (M) e o volume (V), satisfaz:
| \rho \equiv\displaystyle\frac{ M }{ V } |
Isso nos leva a la densidade no estado i (\rho_i) e la densidade no estado f (\rho_f) como:
| \rho_i T_i = \rho_f T_f |
ID:(8835, 0)
