Energia interna
Storyboard 
A energia interna de um sistema consiste em energia cinética e energia potencial. A energia cinética está associada ao calor e pode ser relacionada às oscilações dos átomos em torno de seus pontos de equilíbrio. Por outro lado, a energia potencial está associada ao trabalho que o sistema é capaz de realizar.
ID:(1469, 0)
Mecanismos
Definição 
A energia interna é a energia total contida em um sistema termodinâmico devido às energias cinética e potencial de suas moléculas. Ela inclui a energia proveniente do movimento molecular (translacional, rotacional e vibracional) e a energia das interações intermoleculares e das ligações químicas. A energia interna é uma função de estado, o que significa que depende apenas do estado atual do sistema e não de como o sistema alcançou esse estado. As mudanças na energia interna ocorrem quando calor é adicionado ou removido do sistema ou quando trabalho é realizado sobre ou pelo sistema. Este conceito é fundamental na termodinâmica, descrevendo as mudanças de energia em processos como processos isotérmicos, adiabáticos, isobáricos e isocóricos. A energia interna ajuda a determinar os estados de equilíbrio e a estabilidade do sistema, já que os sistemas tendem a se mover para estados com menor energia interna. Ela fornece uma medida abrangente de todas as formas microscópicas de energia dentro de um sistema, essencial para entender as transformações de energia em diversos processos.
ID:(15245, 0)
Energia cinética
Imagem 
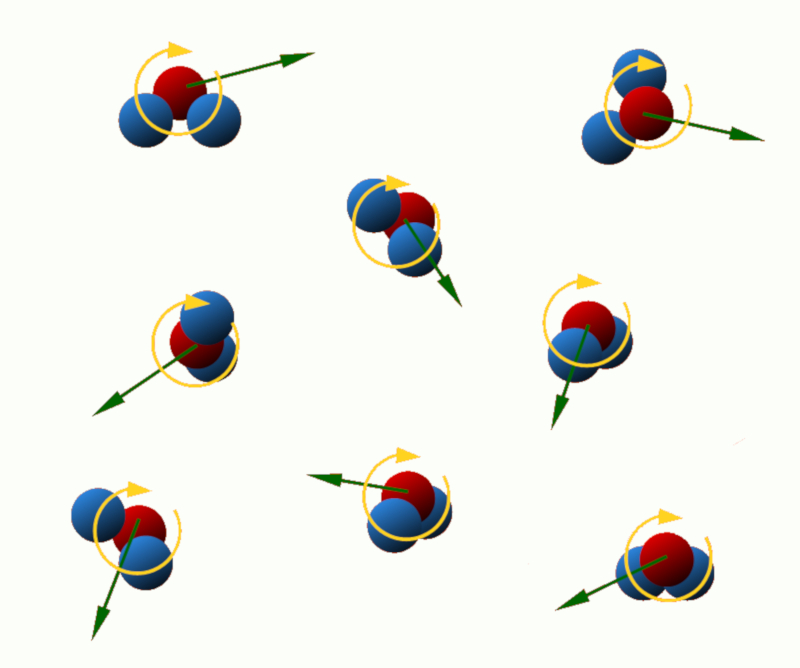
Energia cinética de translação: Essa energia está associada ao movimento linear das partículas no sistema. Quanto maior a velocidade de translação das partículas, maior a sua energia cinética de translação.
Energia cinética de rotação: Algumas partículas, como átomos ou moléculas, podem girar em torno de um eixo. Essa rotação está associada à energia cinética de rotação, que depende da massa e da velocidade angular das partículas.
ID:(11122, 0)
Energia de ligação
Nota 
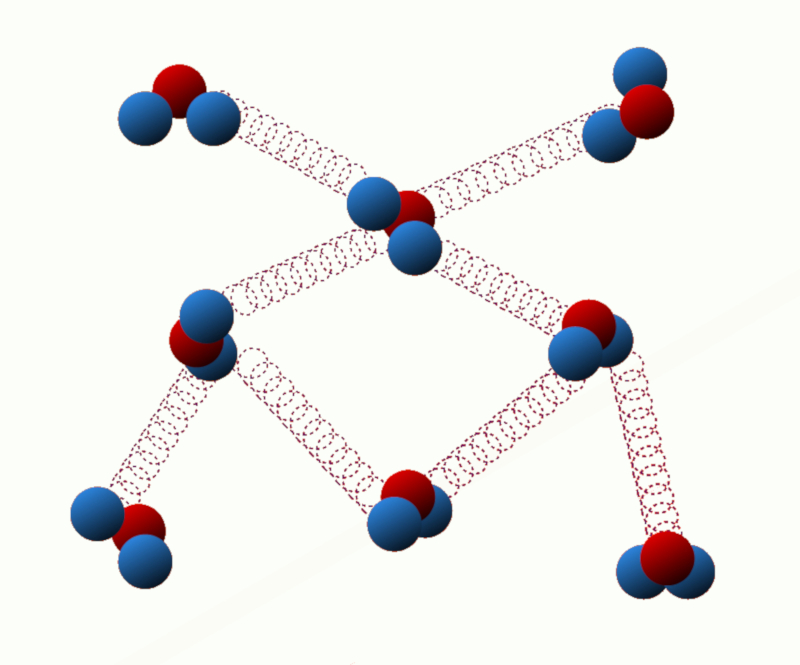
Energia potencial de ligação: Essa energia está relacionada às forças de interação entre as partículas do sistema. Por exemplo, em um sólido, a energia de ligação é devido às forças de atração entre átomos ou moléculas vizinhas.
ID:(11123, 0)
Energia química
Citar 
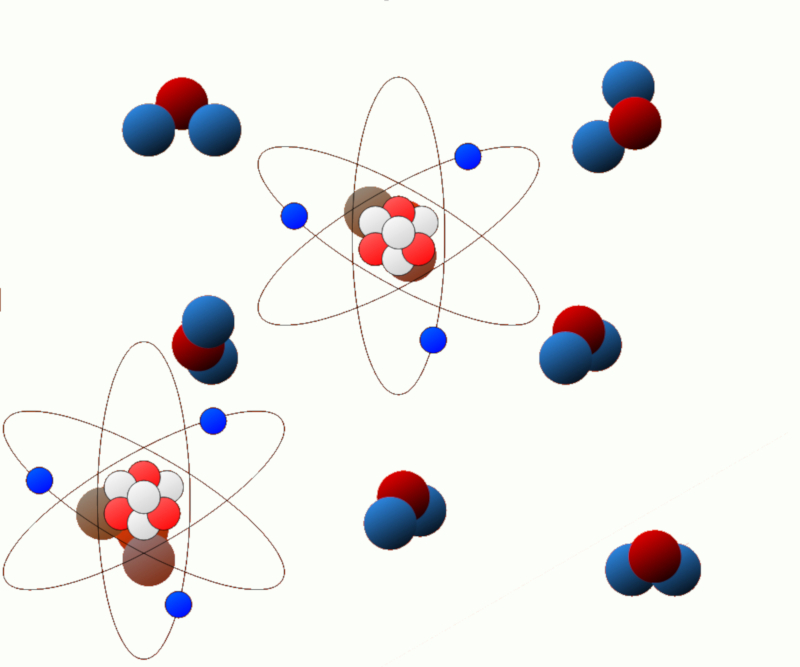
Energia de excitação: Alguns sistemas podem sofrer mudanças em seu estado energético, como quando elétrons em um átomo ou molécula são excitados. A energia associada a esses estados excitados é conhecida como energia de excitação.

ID:(11124, 0)
Energia de excitação
Exercício 
Energia química (energia elétrica): Em sistemas químicos, reações químicas podem liberar ou absorver energia. Essa energia é conhecida como energia química e está relacionada às ligações químicas presentes nas moléculas.
ID:(11125, 0)
Energia interna
Equação 
A energia interna é a energia total possuída pelas partículas que compõem um sistema. Essas energias incluem:
• Energia cinética de translação: Essa energia está associada ao movimento linear das partículas no sistema. Quanto maior a velocidade de translação das partículas, maior a sua energia cinética de translação.
• Energia cinética de rotação: Algumas partículas, como átomos ou moléculas, podem girar em torno de um eixo. Essa rotação está associada à energia cinética de rotação, que depende da massa e da velocidade angular das partículas.
• Energia potencial de ligação: Essa energia está relacionada às forças de interação entre as partículas do sistema. Por exemplo, em um sólido, a energia de ligação é devido às forças de atração entre átomos ou moléculas vizinhas.
• Energia química (energia elétrica): Em sistemas químicos, reações químicas podem liberar ou absorver energia. Essa energia é conhecida como energia química e está relacionada às ligações químicas presentes nas moléculas.
• Energia de excitação: Alguns sistemas podem sofrer mudanças em seu estado energético, como quando elétrons em um átomo ou molécula são excitados. A energia associada a esses estados excitados é conhecida como energia de excitação.
ID:(11121, 0)
