Salzauflösung im Ozean
Bild 
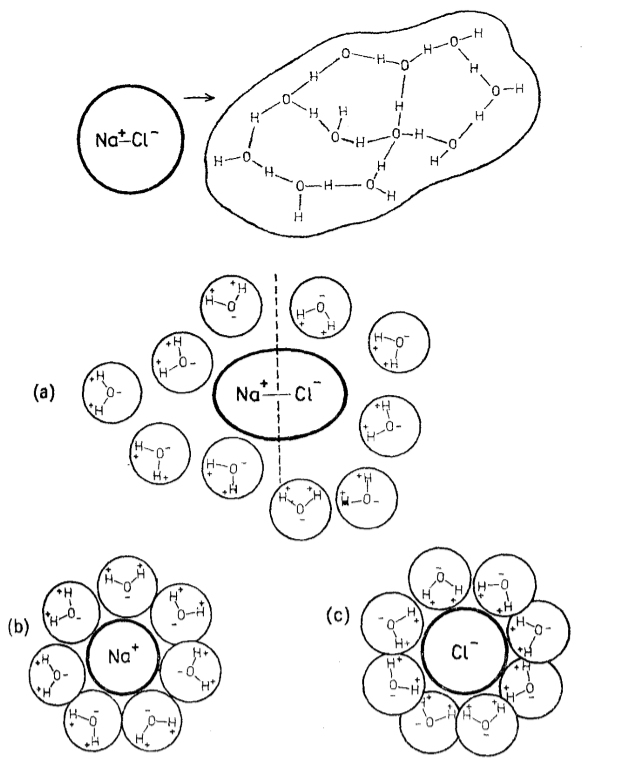
Die Ionen im Salz dissoziieren und sind von Wassermolekülen umgeben, die Cluster bilden, die größer sind als das ursprüngliche Ion:
ID:(11991, 0)
Salzionenhydrat
Bild 
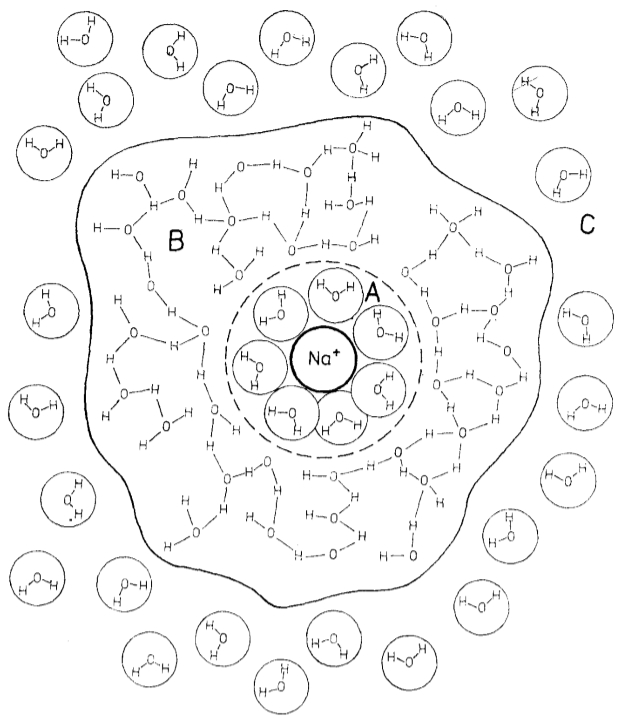
Sobald das Ion von Wassermolekülen umgeben ist, wird eine zweite Schicht von Molekülen gebildet, die durch Brücken verbunden sind:
ID:(11992, 0)
Elektrische Feld wirkt auf das Ionenhydrat des Salzes
Bild 
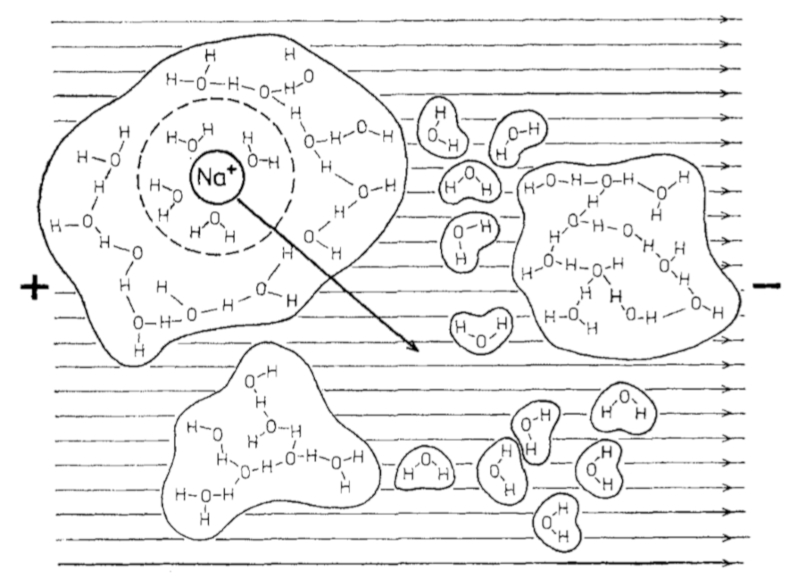
Wenn ein elektrisches Feld an Wasser mit Salzionen angelegt wird, beginnen sich diese in Richtung der positiven Pole zu bewegen:
ID:(11993, 0)
Elektrische Leitfähigkeit als Funktion des Salzgehalts
Bild 
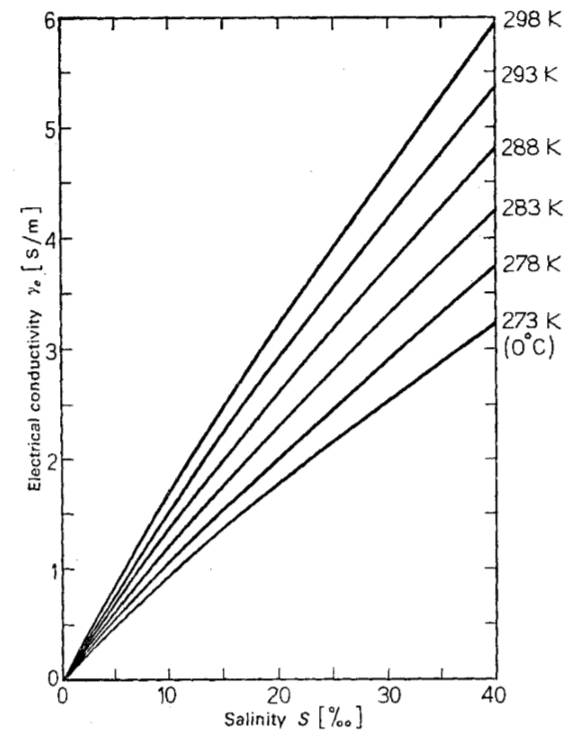
Die elektrische Leitfähigkeit als Funktion von Salzgehalt und Temperatur erklärt sich durch das größere Vorhandensein von Ionen und die größere Mobilität bei höheren Temperaturen:
ID:(11994, 0)
Elektrische Leitfähigkeit als Funktion des Drucks
Bild 
Elektrische Leitfähigkeit in Abhängigkeit von Druck und Temperatur:

ID:(11995, 0)
Spezifische Leitfähigkeitsmessung von Meerwasser
Gleichung 
Die in Meerwasser unter atmosphärischem Druck gemessene spezifische Leitfähigkeit kann empirisch dargestellt werden als
| \gamma_e = a T + b S + c T S + d |
ID:(11999, 0)
Werte der elektrischen Leitfähigkeit als Funktion des Salzgehalts
Bild 
Die folgende Tabelle zeigt die elektrische Leitfähigkeit als Funktion des Salzgehalts:

ID:(11996, 0)
Medición de salinidad
Gleichung 
Dado que la resistencia del agua marina depende de su salinidad, se puede medir la resistencia para determinar el nivel de salinidad. Esto se hace comparando las conductividades de una muestra de agua marina con una solución standard de KCl (clorato de potasio). Se miden la conductividad especifica de ambas muestras a una temperatura de 15C y 1 atm de presión y establece la relación\\n\\n
K=\sqrt{\displaystyle\frac{\gamma_w}{\gamma_{KCl}}}
y calcula la salinidad con
| S = a_0 + a_1 K + a_2 K^2 + a_3 K^3 + a_4 K^4 + a_5 K^5 |
con
a_0=0.0080
a_1=-0.1692
a_2=25.3851
a_3=14.0941
a_4=-7.0261
a_5=2.7081
ID:(12424, 0)
