Convección
Storyboard 
La diferencia de presión atmosférica lleva a desplazamiento de masas de aire tanto a nivel de superficie como en las alturas.
El flujo vertical se denomina convección y es clave para la formación de nubes, generación de lluvias y flujo efectivo de energía entre superficie y atmósfera.
ID:(552, 0)
Convección
Descripción 
Al calentarse una masa de aire esta tiende a dilatarse reduciendose su densidad.
La expansión en si crea una situación en que la presión en su parte superior es menor que en su parte inferior lo que da origen a una diferencia de presión y con ello a una fuerza.
Esta fuerza es analoga a la fuerza de sustentación en el agua, con la diferencia de que con la altura se va reduciendo hasta el punto que ya no supera la gravedad y el cuerpo no continua acendiendo.
ID:(40, 0)
Número de Rayleigh
Ecuación 
El inicio de convección térmica esta descrito por el número de Rayleigh que incluye una serie de parámetros propios del aire y otros geométricos de la situación
| Ra=\displaystyle\frac{\rho^2 g c_p}{\eta\lambda}\displaystyle\frac{(T_e-T_t)}{T_e}h^3 |
y que permite determinar cuando la situación se vuelve inestable.
Para un sistema entre dos placas con las temperaturas inferior
En el caso de corrientes aéreas la densidad es
por lo que con el gradiente
se concluye que prácticamente siempre de tiene las condiciones para que exista convección.
ID:(9040, 0)
Aerodinámica de la convección
Ecuación 
En general el flujo del aire se puede modelar mediante la ecuación de Navier Stokes
| \rho v\displaystyle\frac{dv}{dx}=(\rho_m-\rho) g |
que en el caso de un flujo unidimensional en una dimensión se puede escribir como
| \rho v\displaystyle\frac{dv}{dx}=(\rho_m-\rho) g |
donde
Si la velocidad inicial es cero la integración de la ecuación nos dará
| v(z)^2=2g\displaystyle\int_0^zds\displaystyle\frac{(\rho_m(s)-\rho(s))}{\rho(s)} |
ID:(9938, 0)
Ecuación de Navier Stokes
Ecuación 
El flujo de un liquido o gas es descritos mediante la ecuación de Navier Stokes
| \rho\left(\displaystyle\frac{\partial\vec{u}}{\partial t}+\vec{u}\cdot\nabla\vec{u}\right)=-\nabla p+\eta\nabla^2\vec{u}+\displaystyle\frac{1}{3}\nabla(\nabla\cdot\vec{u})+\rho\vec{g} |
que en la aproximación de baja viscosidad, una situación que se puede modelar dimensional y es un flujo estacionario se reduce a
El gradiente de la presión se modela en este caso con la presión barométrica dando
| \rho v\displaystyle\frac{dv}{dx}=(\rho_m-\rho) g |
ID:(9937, 0)
Velocidad de ascenso
Ecuación 
Para el caso de que la masa de aire asciende en forma lenta la ecuación hidrodinámica de Navier Stokes en una dimensión se puede escribir como
| \rho v\displaystyle\frac{dv}{dx}=(\rho_m-\rho) g |
donde
Si la velocidad inicial es cero la integración de la ecuación nos dara
| v(z) ^2 = 2 g \displaystyle\int_0^zds\displaystyle\frac{( \rho_m(s) - \rho(s) )}{ \rho(s) } |
ID:(4869, 0)
CAPE
Ecuación 
Como la densidad es proporcional al inverso de la temperatura
se tiene que el factor
en
| v(z) ^2 = 2 g \displaystyle\int_0^zds\displaystyle\frac{( \rho_m(s) - \rho(s) )}{ \rho(s) } |
se puede reemplazar por
e introducir
| CAPE=g\displaystyle\int_0^z ds\displaystyle\frac{(T(s)-T_m(s))}{T_m(s)} |
que tiene unidades de energía y corresponde a la energía potencial de convección CAPE.
ID:(9923, 0)
Velocidad de ascenso en función del CAPE
Ecuación 
Con la velocidad de ascenso dada por
| v(z) ^2 = 2 g \displaystyle\int_0^zds\displaystyle\frac{( \rho_m(s) - \rho(s) )}{ \rho(s) } |
y la definición del CAPE
| CAPE=g\displaystyle\int_0^z ds\displaystyle\frac{(T(s)-T_m(s))}{T_m(s)} |
se tiene que la velocidad de ascenso en función del CAPE es
| v =\sqrt{2 CAPE } |
ID:(8836, 0)
Energía potencial de convección
Imagen 
El proceso de convección se describe con el diagrama de presión y temperatura en que se diagraman
- la adiabata de aire seco
- la adiabata de aire humedio
- la temperatura ambiental
y se determina como el volumen evolucionara:
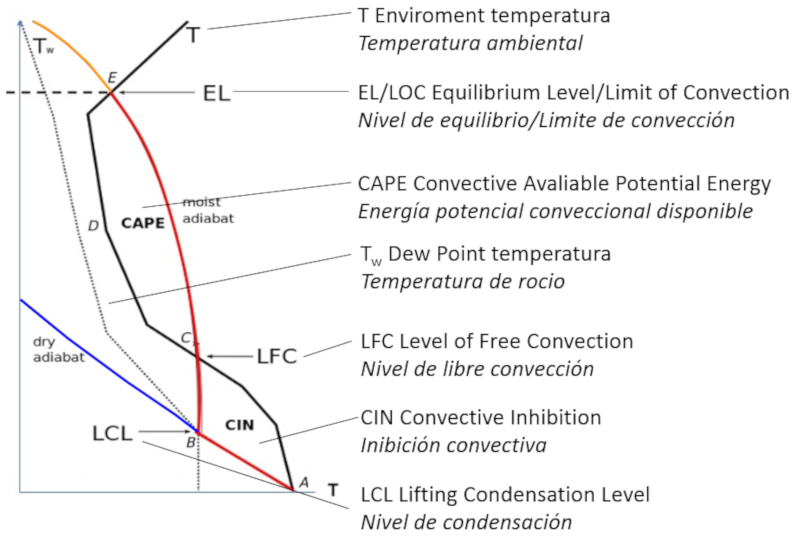
Diagrama de CAPE (Energía potencial de convección disponible)
En el diagrama se muestra como la masa de aire sube:
- sin condesar desde A a B donde inicia la condensación
- comienza a condesar y sube de B a C contra la resistencia CIN
- continua subiendo de C a D impulsado por la energía potencial de condensación
La fase CIN puede evitar que la masa sufra la convección y vuelva a decender.
ID:(3098, 0)
Coeficiente adiabático para aire seco
Ecuación 
Para un proceso adiabático el trabajo es
con
que para un gas ideal es 5/3. De la primera ley de la termodinámica se tiene que
Como en el caso de la atmósfera es
se tiene que el gradiente adiabático es
para el caso del aire seco es
| \Gamma=\displaystyle\frac{g}{c_p} |
que corresponde a 9.8 C/km.
ID:(9924, 0)
Relación de masas molares vapor de agua con aire
Ecuación 
La relación de masas molares del vapor de agua con el aire se define como la relación de las masas molares de cada componente presentes en un volumen:
| \zeta=\displaystyle\frac{M_{mol,v}}{M_{mol,a}} |
Como los valores son fijos se puede estimar el valor, el que resulta ser igual a
ID:(9925, 0)
Relación de mezcla de vapor de agua con aire
Ecuación 
La relación de mezcla del vapor de agua con el aire se define como la relación de las masas de cada componente presentes en un volumen:
\displaystyle\frac{M_v}{M_a}=\displaystyle\frac{n_vM_{mol,v}}{n_aM_{mol,a}}=\displaystyle\frac{p_v}{p_a}\displaystyle\frac{M_{mol,v}}{M_{mol,a}}\sim 0.01
Donde M_v y M_a son las masas de vapor de agua y aire respectivamente, n_v y n_a son las moles de vapor de agua y aire, M_{mol,v} y M_{mol,a} son las masas molares de vapor de agua y aire, p_v y p_a son las presiones relativas de vapor de agua y aire, y r es la relación de mezcla. Por ello se tiene que es
En el caso específico del vapor de agua en el aire, la relación de mezcla es proporcional a las presiones relativas, que se pueden cuantificar utilizando la presión de vapor de agua p_v\sim 1500 Pa y la presión del aire p_a\sim 10^5 Pa. Al aplicar la ecuación de los gases y la definición de la masa molar, se obtiene que la relación de mezcla es aproximadamente 0.01. Esto significa que la cantidad de vapor de agua en comparación con el aire es baja en condiciones normales.
ID:(7069, 0)
Relación de mezcla de vapor de agua con aire en moles
Ecuación 
Con la relación de mezcla de vapor de agua en función de la masa:
| r =\displaystyle\frac{ M_v }{ M_a } |
la relación entre moles y masas
| n = \displaystyle\frac{ M }{ M_m } |
y la relación entre masas molares
| \zeta=\displaystyle\frac{M_{mol,v}}{M_{mol,a}} |
se obtiene la relación de mezcla de vapor de agua con aire en función de los moles
| \displaystyle\frac{n_v}{n_a}=\displaystyle\frac{r}{\zeta} |
ID:(9933, 0)
Variaciones de calor para aire húmedo
Ecuación 
La variación del calor esta para aire seco:
| \Delta Q = C_p \Delta T |
Para el caso de aire húmedo debe considerarse también la masa del vapor de agua. Como la proporción de masa es
| r =\displaystyle\frac{ M_v }{ M_a } |
se tiene que la masa se puede escribir como
donde
| \delta Q = M_a(1+ r ) c_p dT |
ID:(9927, 0)
Variaciones de trabajo para aire húmedo
Ecuación 
La variación del trabajo esta para aire seco:
| \delta W = p dV |
Para el caso de aire húmedo debe considerarse los moles del vapor de agua. Con la ecuación de los gases
| p V = n R T |
se puede definir el numero total de moles en función de los moles del aire
con lo que la ecuación de estado es
| \delta W=-\left(1+\displaystyle\frac{r}{\zeta}\right)n_aRT\displaystyle\frac{dV}{V} |
ID:(9928, 0)
Variaciones de temperatura y volumen para aire húmedo
Ecuación 
En el caso del proceso adiabatico
| \delta Q =0 |
Como el calor es para el caso de aire húmedo es:
| \delta Q = M_a(1+ r ) c_p dT |
y el trabajo
| \delta W=-\left(1+\displaystyle\frac{r}{\zeta}\right)n_aRT\displaystyle\frac{dV}{V} |
se obtiene con
| \kappa \equiv1+\displaystyle\frac{ R }{ M_m c_V } |
se obtiene la ecuación de estado
| \displaystyle\frac{dT}{T}=-\displaystyle\frac{(1+r/\zeta)}{(1+r)}(\kappa-1)\displaystyle\frac{dV}{V} |
Al ser
ID:(9926, 0)
Variación del vapor por condensación
Ecuación 
En el caso de que el aire esta saturado, la presión del vapor de agua es:
| p_s = p_{ref} e^{- l_m / R T } |
y con la ecuación de los gases expresada en función de la concentración
| p = c_m R T |
se obtiene que
Si la temperatura varia en una pequeña cantidad
Como el calor latente del agua es del orden de
| dc_s=c_s\displaystyle\frac{l_m}{RT^2}dT |
ID:(9929, 0)
Variación del vapor por condensación en función de la masa
Ecuación 
Como la concentración varia con la temperatura en primer orden como:
| dc_s=c_s\displaystyle\frac{l_m}{RT^2}dT |
y la concentración se define como
| c_m \equiv\displaystyle\frac{ n }{ V } |
se concluye con
| n = \displaystyle\frac{ M }{ M_m } |
que la variación de la masa es
| dM_s=M_s\displaystyle\frac{l_m}{RT^2}dT |
ID:(9934, 0)
Factor de mezcla para el caso saturado
Ecuación 
Al estar saturado el ractor de mezcla
| r =\displaystyle\frac{ M_v }{ M_a } |
se debe calcular con la masa saturada que se puede obtener de la concentración saturada multiplicando por el volumen y la masa molar
Como por el otro lado la masa del aire es
se obtiene que la relación de mezclado del vapor de agua saturado es
| r_s=\zeta_s\displaystyle\frac{p_0}{p_a}e^{-l_m/RT} |
ID:(9935, 0)
Variaciones de calor para aire saturado
Ecuación 
La variación del calor esta para aire seco:
| \Delta Q = C_p \Delta T |
Para el caso de aire saturado debe considerarse que la variación del vapor de agua lleva al aumento de la masa saturada la que aumenta según
| dM_s=M_s\displaystyle\frac{l_m}{RT^2}dT |
y que entrega el calor que se obtiene multiplicando este valor por el calor latente
Como ademas la masa del vapor de agua se puede relacionar con la masa de aire por la relación de mezcla
| r =\displaystyle\frac{ M_v }{ M_a } |
se concluye que el calor se modifica con la variación de la temperatura como
| \delta Q = M_a\left(c_p+\displaystyle\frac{l_m^2r_s}{RT^2}\right)dT |
donde la relación de mezcla es
| r_s=\zeta_s\displaystyle\frac{p_0}{p_a}e^{-l_m/RT} |
ID:(9931, 0)
Variaciones de trabajo para aire saturado
Ecuación 
La variación del trabajo esta para aire seco:
| \delta W = p dV |
Para el caso de aire saturado debe considerarse que la variación del vapor de agua lleva al aumento de la concentración saturada la que aumenta según
| dc_s=c_s\displaystyle\frac{l_m}{RT^2}dT |
con lo que la ecuación de estado es
| \delta W=-\left(1+\displaystyle\frac{l_mr_s}{RT}\right)n_aRT\displaystyle\frac{dV}{V} |
donde la relación de mezcla es
| r_s=\zeta_s\displaystyle\frac{p_0}{p_a}e^{-l_m/RT} |
ID:(9930, 0)
Variaciones de temperatura y volumen para aire saturado
Ecuación 
En el caso del proceso adiabatico
| \delta Q =0 |
Como el calor es para el caso de aire húmedo es:
| \delta Q = M_a\left(c_p+\displaystyle\frac{l_m^2r_s}{RT^2}\right)dT |
y el trabajo
| \delta W=-\left(1+\displaystyle\frac{l_mr_s}{RT}\right)n_aRT\displaystyle\frac{dV}{V} |
se obtiene con
| \kappa \equiv1+\displaystyle\frac{ R }{ M_m c_V } |
se obtiene la ecuación de estado
| \displaystyle\frac{dT}{T}=-\displaystyle\frac{\left(1+\displaystyle\frac{l_mr_s}{RT}\right)}{\left(1+\displaystyle\frac{l_m^2r_s}{c_pRT^2}\right)}(\kappa-1)\displaystyle\frac{dV}{V} |
Si se evalua el factor que se antepone a el factor
ID:(9932, 0)
Coeficiente adiabático para aire saturado
Ecuación 
Para el caso del aire no saturado el gradiente adiabático era
| \Gamma=\displaystyle\frac{g}{c_p} |
que con la ecuación del proceso adiabatico saturado
| \displaystyle\frac{dT}{T}=-\displaystyle\frac{\left(1+\displaystyle\frac{l_mr_s}{RT}\right)}{\left(1+\displaystyle\frac{l_m^2r_s}{c_pRT^2}\right)}(\kappa-1)\displaystyle\frac{dV}{V} |
con lo que el coeficiente adiabático para aire saturado es
| \Gamma=\displaystyle\frac{g}{c_p}\displaystyle\frac{1+\displaystyle\frac{l_mr_s}{RT}}{1+\displaystyle\frac{l_m^2r_s\epsilon}{c_pRT^2}} |
El valor se puede representar como el coeficiente adiabático no saturado multiplicado por un coeficiente que es del orden de 0.55. De esta forma el coeficiente adiabático de aire saturado es del orden de 5.4 C/km.
ID:(3097, 0)
