Constante de Rydberg
Ecuación
La constante de Rydberg se puede calcula de las constantes fundamentales $e$ carga del electrón, $m$ la masa del electrón, $\epsilon_0$ la constante de campo y $h$ la constante de Planck
| $Ry=\displaystyle\frac{e^4m}{8\epsilon_0^2h^2}$ |
La unidad eV $($Electrón Volt$)$ corresponde a la energía que requiere un electrón para desplazarlo entre dos placas a una diferencia de $1 V$ por $1 m$ lo que son $1.6\times 10^{19}J$.
ID:(3956, 0)
Energía de un Orbital
Ecuación
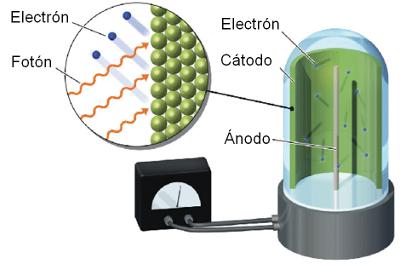
De igual forma un fotón puede ser absorbido por un electrón permitiendo que pase a una órbita mas lejana al núcleo. Nils Bohr fue el que logro modelar estos procesos de excitación y des-excitación usando su modelo del átomo como sistema planetario.
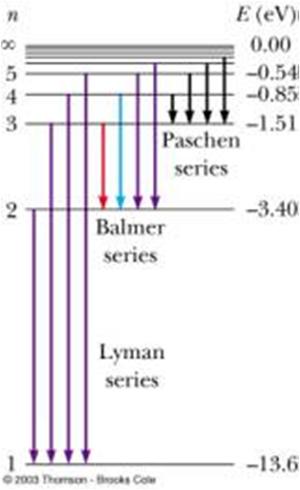
La energía de la banda es una función de la constante de Rydberg $Ry$, numero de protones $Z$ del núcleo y $n$ el nivel
| $E_n=-\displaystyle\frac{RyZ^2}{n^2}$ |
ID:(3955, 0)
Frecuencia del Photon al Saltar Electrones entre Orbitales
Ecuación
Cada vez que un electrón cae de una orbita $n$ a una órbita $m$ mas cercana al núcleo emite un fotón de frecuencia $
u$ una energía $h
u$ igual a la diferencia de las energías $E_n$ y $E_m$ entre los dos niveles:
| $h\nu=E_n-E_m$ |
ID:(3954, 0)
Frecuencia y Largo de Onda de Fotónes
Ecuación
El fotón se describe como una onda, y la frecuencia $
u$ se relaciona con la longitud de onda $\lambda$ mediante la velocidad de la luz $c$, de acuerdo con la siguiente fórmula:
Dado que la frecuencia es el inverso del período de una oscilación:
$\nu=\displaystyle\frac{1}{T}$
esto significa que la velocidad de la luz es igual a la distancia recorrida en una oscilación, es decir, la longitud de onda, dividida por el tiempo transcurrido, que es el período:
$c=\displaystyle\frac{\lambda}{T}$
En otras palabras:
| $ c = \nu \lambda $ |
Esta fórmula corresponde a la relación de la mecánica que establece que la velocidad es igual al espacio recorrido (longitud de onda) dividido por el tiempo transcurrido (la frecuencia es el inverso del periodo).
ID:(3953, 0)