Primeira Lei da Termodinâmica
Storyboard 
A primeira lei da termodinâmica estabelece que a energia é conservada e consiste em duas partes: uma associada ao trabalho e outra ao calor. Diferentemente do trabalho, esta última parte não pode ser completamente convertida em trabalho, o que limita as conversões energéticas possíveis.
ID:(1398, 0)
Pressão e trabalho
Citar 
Consideremos um gás em um cilindro onde um pistão pode se deslocar. Se o pistão for movido, é possível reduzir o volume, comprimindo o gás. Para realizar essa compressão, é necessária uma energia que é igual à força exercida pelo gás multiplicada pela distância percorrida pelo pistão. Essa energia também pode ser representada em função da pressão, já que a pressão é definida pela força e pela área do pistão.
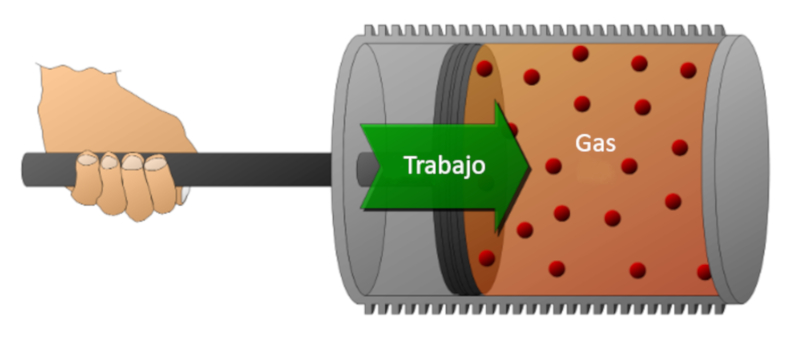
O trabalho pode ser realizado pelo sistema (compressão) ou pelo sistema sobre o meio externo (expansão).
Uma vez que la força mecânica ($F$) dividido por la seção ($S$) é igual a la pressão ($p$):
| $ p \equiv\displaystyle\frac{ F }{ S }$ |
e la variação de volume ($\Delta V$) com o distância percorrida ($dx$) é igual a:
| $ \Delta V = S \Delta s $ |
A equação para o diferencial de trabalho impreciso ($\delta W$) pode ser expressa como:
| $ \delta W = F dx $ |
Portanto, ela pode ser escrita como:
| $ \delta W = p dV $ |
ID:(11126, 0)
Primeira Lei da Termodinâmica
Descrição 
A primeira lei da termodinâmica estabelece que a energia é conservada e consiste em duas partes: uma associada ao trabalho e outra ao calor. Diferentemente do trabalho, esta última parte não pode ser completamente convertida em trabalho, o que limita as conversões energéticas possíveis.
Variáveis
Cálculos
Cálculos
Equações
(ID 3202)
Uma vez que la força mecânica ($F$) dividido por la seção ($S$) igual a la pressão ($p$):
| $ p \equiv\displaystyle\frac{ F }{ S }$ |
e la variação de volume ($\Delta V$) com o distância percorrida ($dx$) igual a:
| $ \Delta V = S \Delta s $ |
A equa o para o diferencial de trabalho impreciso ($\delta W$) pode ser expressa como:
| $ \delta W = F dx $ |
Portanto, ela pode ser escrita como:
| $ \delta W = p dV $ |
(ID 3468)
(ID 3469)
Uma vez que o diferencial de energia interna ($dU$) est relacionado com o diferencial de calor impreciso ($\delta Q$) e o diferencial de trabalho impreciso ($\delta W$) da seguinte forma:
| $ dU = \delta Q - \delta W $ |
E sabido que o diferencial de trabalho impreciso ($\delta W$) est relacionado com la pressão ($p$) e la variação de volume ($\Delta V$) como segue:
| $ \delta W = p dV $ |
Portanto, podemos concluir que:
| $ dU = \delta Q - p dV $ |
(ID 3470)
(ID 15700)
(ID 15701)
Exemplos
A primeira lei da termodin mica, tamb m conhecida como lei da conserva o da energia, afirma que a energia n o pode ser criada nem destru da em um sistema isolado; ela pode apenas ser transferida ou transformada. Esse princ pio estabelece que a energia total de um sistema isolado permanece constante. Em termos pr ticos, isso significa que a mudan a na energia interna de um sistema igual ao calor adicionado ao sistema menos o trabalho realizado pelo sistema. A energia interna abrange a energia total dentro de um sistema, incluindo a energia cin tica e potencial a n vel molecular. O calor a energia transferida entre sistemas devido a uma diferen a de temperatura, enquanto o trabalho a energia transferida quando uma for a aplicada sobre uma dist ncia, frequentemente relacionada a mudan as de volume em gases. A primeira lei fundamental para analisar a efici ncia de motores t rmicos, o desempenho de sistemas de refrigera o e aquecimento e para entender processos metab licos em sistemas biol gicos. Ela fornece uma base para compreender as transfer ncias e transforma es de energia em v rios processos f sicos, garantindo que a energia dentro de um sistema isolado seja sempre conservada.
(ID 15250)
A primeira lei da termodin mica estabelece que a energia sempre conservada.
Enquanto na mec nica existe uma conserva o similar, restrita a sistemas n o dissipativos (por exemplo, excluindo o atrito), na termodin mica essa lei generalizada, considerando n o apenas o trabalho mec nico, mas tamb m o calor gerado ou absorvido pelo sistema.
Nesse sentido, a conserva o de energia postulada na termodin mica n o possui restri es e aplic vel a todos os sistemas, desde que sejam consideradas todas as trocas e convers es de energia poss veis.
(ID 37)
Consideremos um g s em um cilindro onde um pist o pode se deslocar. Se o pist o for movido, poss vel reduzir o volume, comprimindo o g s. Para realizar essa compress o, necess ria uma energia que igual for a exercida pelo g s multiplicada pela dist ncia percorrida pelo pist o. Essa energia tamb m pode ser representada em fun o da press o, j que a press o definida pela for a e pela rea do pist o.

O trabalho pode ser realizado pelo sistema (compress o) ou pelo sistema sobre o meio externo (expans o).
Uma vez que la força mecânica ($F$) dividido por la seção ($S$) igual a la pressão ($p$):
| $ p \equiv\displaystyle\frac{ F }{ S }$ |
e la variação de volume ($\Delta V$) com o distância percorrida ($dx$) igual a:
| $ \Delta V = S \Delta s $ |
A equa o para o diferencial de trabalho impreciso ($\delta W$) pode ser expressa como:
| $ \delta W = F dx $ |
Portanto, ela pode ser escrita como:
| $ \delta W = p dV $ |
(ID 11126)
(ID 15309)
ID:(1398, 0)
